





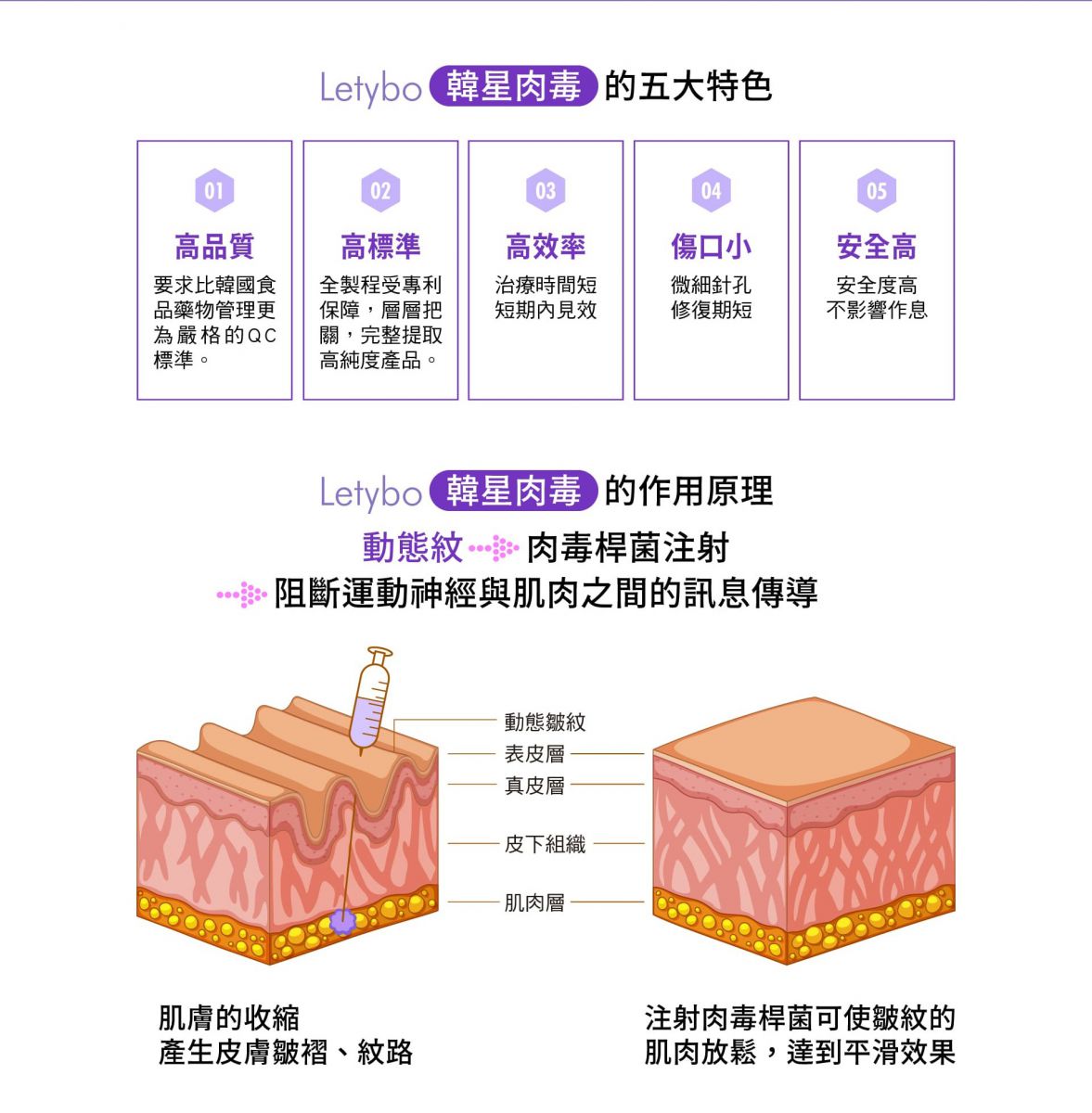



適應症
暫時性改善因皺眉肌及(或)鼻眉肌活躍而出現之中度至重度皺眉紋。
注意事項
1. 警告事項
由於本產品的活性成分 A 型肉毒桿菌毒素是由肉毒桿菌所產生,應完全瞭解施用的注意事項,並嚴格遵守建議的施用方
法和劑量。施用本產品的醫師必須充分瞭解相關部位的神經肌肉和眼窩的解剖結構,以及因之前的手術對解剖結構的任
何改變。
另外也必須瞭解標準的肌電圖(EMG)技術。不可超過建議劑量和施用頻率。
(1) 毒素作用的遠端轉移:肉毒桿菌毒素可能會從注射部位轉移至其他部位而產生副作用。可能會發生的症狀包括虛
弱、全身性肌肉無力、發音困難、言語障礙、口吃、膀胱失禁、呼吸困難、吞嚥困難、視力重疊、視力模糊和眼
瞼下垂。吞嚥困難或呼吸困難可能會危及生命。過去曾經有過毒素轉移導致死亡的案例。用於治療患有腦性麻痺
痙攣的兒童的風險特別大,但是相同的症狀也會發生於治療腦性麻痺痙攣或其他疾病的成人。以上的不良反應也
曾發生於以治療斜頸症的劑量或更低劑量的患者。
3
(2) 過敏性反應:嚴重和(或)立即的過敏性反應曾被報導於其他肉毒桿菌毒素產品。這些反應包括急性過敏、蕁麻疹、
軟組織水腫和呼吸困難。有一個急性過敏的案例是使用利度卡因(lidocaine)當作稀釋劑,但是致病劑尚未清楚確定。
如果在注射本產品後發生過敏性反應,應停止繼續注射本產品,並立即進行適當的治療。
(3) 預先存在的神經肌肉障礙:在罹患周邊運動神經系統疾病(如肌萎縮性脊隨側索硬化症、運動神經病變)或神經肌肉
接合疾病(如重症肌無力或藍伯‒伊頓肌無力症)的患者中,即使注射肉毒桿菌毒素的一般治療劑量,明顯的全身性
反應的風險仍可能會增加,包括嚴重吞嚥和呼吸困難。依據其他肉毒桿菌毒素產品的臨床文獻,在可識別或不可
識別的神經肌肉疾病患者中,少見有因肉毒桿菌毒素的一般治療劑量所引起的全身性嚴重過敏性反應。在某些病
例中,由於吞嚥困難持續好幾個月,因此必須使用胃管餵食。
(4) 吞嚥困難:使用肉毒桿菌毒素治療斜頸症的患者時,吞嚥困難是常見的不良反應。在某些罕見的情況下,罹患嚴
重吞嚥困難的患者必須以胃管餵食。曾經有發生吞嚥困難後產生吸入性肺炎致死的案例。
(5) 有報導指出在施用其他肉毒桿菌毒素產品後導致的心血管疾病的不良反應,包括心律不整和心肌梗塞,但是某些
病例會致死。其中有些患者本來已有心血管疾病的風險因子。
(6) 利用其他肉毒桿菌產品治療斜視時,由於針穿入眼球周遭,眼球後方可能會發生視網膜出血。建議以適當儀器降
低眼眶壓力。外物穿刺傷害眼球的情形也有可能發生,此時須使用眼底鏡檢查眼睛狀況。一或以上的眼眶外肌肉
發生麻痺可能產生空間迷失、複視或過指情形。遮住眼睛可減緩這些症狀。
(7) 眼瞼痙攣:因肉毒桿菌毒素注射至眼輪匝肌而造成的眨眼次數減少可能導致角膜暴露、持續性角膜上皮缺損及角
膜潰瘍,尤其是第七對腦神經失調患者。使用其他肉毒桿菌毒素產品治療眼瞼痙攣時,曾經發生一無晶狀體眼角
膜穿孔的案例因為此現象而需要進行角膜移植。在執行前必須仔細檢查眼睛角膜知覺和避免注射至下眼瞼以減少
眼瞼外翻的風險。須對角膜上皮缺損進行完整的治療,可能包括保護性藥水、軟膏、治療式軟式隱形眼鏡、使用
眼罩或其他方式遮住眼睛。
(8) 肉毒桿菌產品之間缺乏互換性:由於每個產品的肉毒桿菌毒素效價單位具有特異性,本產品無法與其他肉毒桿菌
毒素產品進行互換。因此,某個肉毒桿菌毒素產品的單位生物活性無法利用其他特殊之評估方法與任何其他肉毒
桿菌毒素產品的單位進行轉換或比較。
(9) 注射於或接近易受傷害解剖位置:注射於或接近易受傷害解剖位置須小心。嚴重不良反應,包含死亡曾經被報導
於使用其他肉毒桿菌毒素產品注射於唾液腺、口舌-咽部位、食道和胃部。有些病患於先前有發生吞嚥困難或虛弱
情形(對於這些部位的適應症並沒有進行安全或有效性評估)。發生於注射期間的氣胸也曾經被報導在使用其他肉毒
桿菌毒素產品注射於胸腔時。注射接近肺臟的相關警語已包含,尤其是肺尖端。
(10) 上肢痙攣或神經疾病相關的逼尿肌過動症患者治療後對肺部與呼吸狀態的影響:上肢痙攣和呼吸道疾病的患者,
曾經被報導比起安慰劑組,發生上呼吸道感染及肺功能下降(肺活量[FVC]下降≥15%)的情況更為頻繁。與神經疾病
相關的逼尿肌過動症患者使用其他肉毒桿菌產品治療後,也曾被報導過有肺功能下降(肺活量[FVC]下降≥15%)及呼
吸困難的情形。
(11) 上肢痙攣患者治療後產生支氣管炎和上呼吸道感染:和安慰劑相比,對施用過其他肉毒桿菌毒素的上肢痙攣患者
而言,支氣管炎是很常被報導的不良反應。而上呼吸道感染在施用肉毒桿菌毒素治療後的伴隨呼吸道功能下降的
上肢痙攣患者,也很常被報導。
4
2. 禁忌症
(1) 對本產品的任何成分過敏的患者
(2) 罹患全身性神經肌肉接合疾病的患者(如重症肌無力、藍伯‒伊頓肌無力症或肌萎縮性脊隨側索硬化症)。這些疾病
可能會因本產品的肌肉鬆弛效果而惡化。
(3) 懷孕或哺乳期的婦女。
一般注意事項
(1) 本產品含有自人體血液取得的白蛋白。施用人體血液或血漿製造的藥物時,無法完全排除傳輸感染疾病的可能性。
這也可能包含未知的病原物質。為了減低傳輸這些感染物質的風險,會對白蛋白的製造過程特別小心,包含病毒
去除和/或滅活程序,並謹慎篩選供體和適當檢測供體濃度。
(2) 本產品對於操作機械或交通工具的影響無法預測,因為相關能力也可能會受到疾病本身的影響。
(3) 皺眉紋:臉部麻痺或眼瞼下垂症狀的病患、建議注射部位有感染、皮膚病徵或疤痕的病患、接受臉部整形手術,
如組織填充、提眉和皮膚表面重建的病患、因其皺眉紋無法以手指撫平而被認為不適合的病患,其狀況無法藉由
實質方法充分改善已於第三期臨床試驗中被排除。本品於皺眉紋的適應症並無重複施打之經驗。本品於眼瞼痙攣
的臨床試驗中,第二次施打的中位數時間為 125 天(平均 125±4.37 天)。建議注射此產品的頻率不高於每四個月一
次,且必須施打最小有效劑量。
使用注意事項
注射前,應使用無防腐劑的無菌生理食鹽水來溶解凍乾的本產品。建議稀釋劑是 0.9%的氯化鈉。將適量的稀釋劑抽
入適當尺寸的注射器。由於泡沫的形成或劇烈的攪動可能會造成本產品變性,稀釋劑需慢慢地將注入小藥瓶。請將稀
釋劑無法因真空而注入的小藥瓶。在標籤上記錄調製日期和時間。調製後的藥物應於 24 小時內施用。調製的溶液應
存放於冷藏狀態(2~8℃)。溶解時,調製的藥物應為清晰無色,且見不到異常物質。在施用前應仔細檢查非口服製劑
是否有異物或變色。由於藥物本身或稀釋劑中都不含任何防腐劑,一個小藥瓶只能使用在一位患者。
本產品韓國臨床試驗結果呈現受試者於注射後皆無產生中和性抗體。
我們可能收集的信息:
我們提供服務時,可能會收集、儲存和使用下列與您有關的信息。如果您不提供相關信息,可能無法註冊成為我們的用戶或無法享受我們提供的某些服務,或者無法達到相關服務擬達到的效果。
您提供的信息:
您在註冊賬戶或使用我們的服務時,向我們提供的相關個人信息,例如電話號碼、電子郵件或銀行卡號等;
您通過我們的服務向其他方提供的共享信息,以及您使用我們的服務時所儲存的信息。
其他方分享的您的信息其他方使用我們的服務時所提供有關您的共享信息。
我們重視用戶的隱私,隱私權是您重要的權利。您在使用我們的服務時,我們可能會收集和使用您的相關信息。我們希望通過本《隱私政策》向您說明,在使用我們的服務時,我們如何收集、使用、儲存和分享這些信息,以及我們為您提供的訪問、更新、控制和保護這些信息的方式。本《隱私政策》與您所使用的其明服務息息相關,希望您仔細閱讀,在需要時,按照本《隱私政策》的指引,作出您認為適當的選擇。本《隱私政策》中涉及的相關技術詞彙,我們盡量以簡明扼要的表述,並提供進一步說明的鏈接,以便您的理解。
您使用或繼續使用我們的服務,即意味著同意我們按照本《隱私政策》收集、使用、儲存和分享您的相關信息。
如對本《隱私政策》或相關事宜有任何問題,請通過service@diamondcosmetic.com.tw 與我們聯繫。